Классификация и свойства электролитов
Электролиты — это вещества, которые при растворении в воде или расплавлении распадаются на ионы и проводят электрический ток. Их способность к диссоциации делает растворы электролитов активными в химических реакциях: ионы легко вступают во взаимодействия, обмениваются зарядами и участвуют в окислительно-восстановительных процессах. К электролитам относят кислоты, основания и соли.
По степени распада их делят на сильные и слабые: сильные диссоциируют почти полностью, а слабые — лишь частично. Свойства электролитов зависят от их природы, концентрации раствора и условий среды, поэтому одни растворы проводят ток хорошо, другие — значительно слабее.
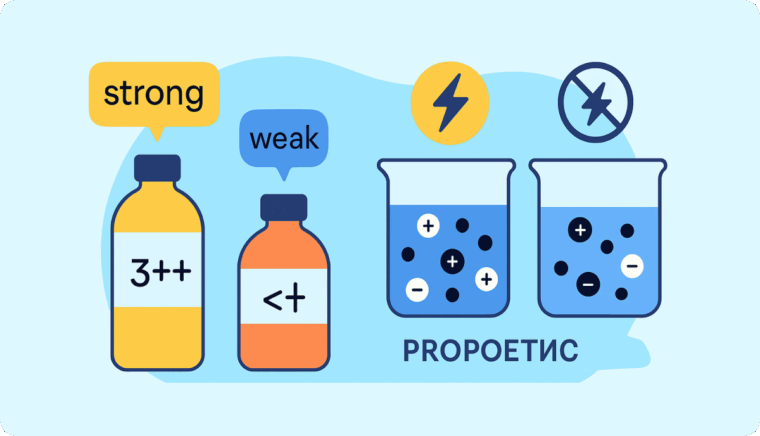
Классификация электролитов
Классификация электролитов строится на том, как именно вещество распадается на ионы и насколько полно проходит этот процесс.
- По природе вещества
Электролиты объединяют три большие группы.
Кислоты — вещества, которые в воде дают катионы водорода и анионы кислотных остатков.
Основания — дают катионы металлов и гидроксид-ионы.
Соли — образуют катионы металлов и анионы кислотных остатков, не содержащие водорода и гидроксид-групп. Эта тройка покрывает основную массу электролитов, встречающихся в химии.
- По силе электролита
Этот признак отражает степень диссоциации, то есть долю частиц, распавшихся на ионы.
Сильные электролиты — почти полностью распадаются в растворе. К ним относят большинство неорганических кислот (например, соляную), растворимые основания и многие соли. Их растворы проводят ток уверенно и равномерно.
Слабые электролиты — диссоциируют частично. Примером служат уксусная кислота или аммиак в воде. В их растворах всегда есть и ионы, и недиссоциированные молекулы, поэтому проводимость ниже.
- По составу и поведению в растворе
Здесь учитывают, какие именно ионы образуются. Простые электролиты дают один тип катиона и один тип аниона. Это типичные соли вроде хлорида натрия.
Сложные электролиты могут образовывать несколько разных ионов или комплексные частицы. Например, комплексные соли диссоциируют ступенчато и дают устойчивые комплексные ионы.
Кроме того, часть веществ диссоциирует по ступеням. Многоосновные кислоты или соли поликарбоновых кислот теряют ионы последовательно, что отражается на силе каждого этапа реакции.
- По агрегатному состоянию
Электролитами могут быть как растворы, так и расплавы. Некоторые твёрдые соли начинают проводить ток только после плавления, когда их кристаллическая решетка разрушается, и ионы становятся подвижными.
дизайну или школьным предметам
одновременно, без доплат!
Запишите ребёнка на бесплатный урок!
Определим его интересы и разработаем гибкий
план обучения.

Свойства электролитов
Растворы электролитов обладают особыми свойствами, которые связаны с присутствием свободных ионов.
- Электропроводность
Главное свойство электролитического раствора — способность проводить электрический ток. Ионы свободно движутся в воде и переносят заряд от электрода к электроду.
Чем выше концентрация и степень диссоциации, тем выше проводимость. Сильные электролиты проводят ток лучше, слабые — хуже.
- Ионные взаимодействия
В растворе одновременно присутствуют катионы и анионы. Они притягиваются, отталкиваются, образуют ионные пары.
Эти процессы влияют на скорость реакций, силу раствора и его общее поведение. В концентрированных растворах такие взаимодействия особенно заметны.
- Осмотическое давление
Растворы электролитов создают более высокое осмотическое давление, чем растворы неэлектролитов при той же концентрации. Это происходит потому, что одна молекула электролита даёт несколько ионов, а значит — больше частиц в растворе.
Осмотическое давление важно для биологических процессов, движений воды через мембраны и регулирования химического равновесия.
- Снижение температуры замерзания и повышение температуры кипения
Эти явления называют коллигативными свойствами. Чем больше частиц в растворе, тем сильнее меняются температуры фазовых переходов. Растворы электролитов дают более заметный эффект, поскольку число частиц увеличивается за счёт диссоциации. Поэтому солёная вода замерзает при более низкой температуре, чем чистая.
- Явления электролитической диссоциации
Растворы электролитов находятся в динамическом равновесии. Молекулы вещества постоянно распадаются на ионы и соединяются обратно. Для слабых электролитов это особенно важно, потому что степень диссоциации зависит от концентрации, температуры и природы растворителя.
- Участие в электрохимических процессах
Электролиты — основа для протекания электролиза. Ионы движутся к электродам, отдают или принимают электроны. Это свойство используют в химической промышленности, гальванике, металлургии.

Составим пошаговый план
по улучшению успеваемости!

