Химические свойства металлов
Химические свойства металлов — это то, как металлы ведут себя в химических реакциях. Проще говоря, что они могут делать при взаимодействии с другими веществами. Например:
- Образуют оксиды.
- Образуют соли и водород.
Что такое металлы?
Большинство химических элементов таблицы Менделеева — это металлы. К ним относятся железо, медь, алюминий, золото, кальций, натрий, магний и многие другие.
Металлы — это большая группа химических элементов, которые имеют общие характерные свойства. Проще говоря, это вещества, которые:
- Хорошо проводят тепло и электричество
Металлическая проволока или ложка быстро нагревается — это из-за высокой проводимости. - Имеют металлический блеск
Они отражают свет, поэтому выглядят блестящими. - Пластичны
Металлы можно тянуть в проволоку, гнуть, раскатывать в лист — они не крошатся. - Преимущественно твердые
Исключение — ртуть, она жидкая при комнатной температуре. - Легко вступают в химические реакции
Они могут реагировать с кислородом, кислотами, водой и другими веществами.
- Читайте также: Все о таблице Менделеева, как с ней работать и выучить
Общие химические свойства металлов
Это типичные реакции, в которые вступает большинство металлов. Они показывают, как металлы ведут себя химически.
- Реакция с кислородом: металлы соединяются с кислородом и образуют оксиды.
Пример: магний + кислород → оксид магния.
- Реакция с кислотами: металлы (кроме самых «благородных») вступают в реакцию с кислотами. Образуются соль и водород.
Пример: цинк + соляная кислота → хлорид цинка + водород.
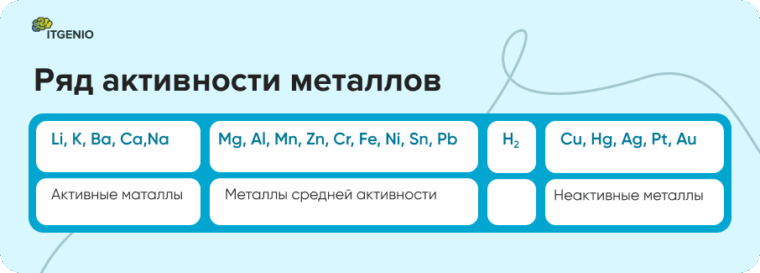
- Реакция с водой: активные металлы (калий, натрий, кальций) реагируют с водой при обычных условиях и дают основания и водород. Менее активные реагируют только при нагревании. Благородные вообще не реагируют.
- Реакция с солями других металлов: металл, который более активен, вытесняет менее активный из его соли.
Пример: железо + медный купорос → медь + раствор соли железа.
- Реакция с неметаллами: металлы легко соединяются с серой, хлором, бромом и другими неметаллами, образуя сульфиды, галогениды и др.

Составим пошаговый план
по улучшению успеваемости!

